'근육 회복 스위치' 역할 단백질 세계 최초 확인
치료제 후보까지 제시
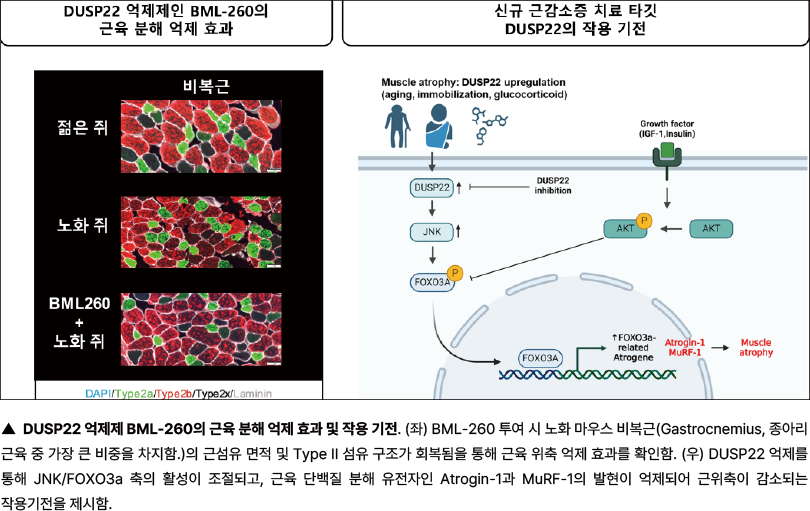
GIST 다런 윌리엄스 교수팀이 근감소증과 노화·약물·사지 고정 등 다양한 근위축 조건에서 핵심 인자로 작용하는 DUSP22 단백질을 세계 최초로 확인했다. 연구팀은 DUSP22를 억제하는 저분자 화합물 BML-260을 활용해 근육량 회복, 근섬유 직경 증가, 근력 개선 등 근기능 회복 효과를 입증하며 근감소증 및 다양한 근육 퇴행성 질환의 치료 가능성을 높였다.
GIST 생명과학과 다런 윌리엄스 교수 연구팀이 노화와 근감소증에서 근육 소실을 유발하는 핵심 인자로 DUSP22 단백질을 확인하고, 이를 억제해 근육 회복을 촉진하는 기술을 개발했다. 연구팀은 근감소증 환자 조직과 노화, 스테로이드 약물, 사지 고정 등 다양한 동물 모델에서 DUSP22 과발현을 관찰했다. 이어 siRNA와 저분자 화합물 BML-260을 활용한 DUSP22 억제 실험에서 근육 위축이 뚜렷하게 완화됨을 입증했다.
BML-260 투여 시 근육 단백질 분해 관련 유전자 Atrogin-1과 MuRF-1 발현이 각각 52%, 57% 감소했으며, 노화 마우스 모델에서는 골격근 무게가 약 26%, 근섬유 직경이 약 25% 회복됐다. 또한 근력은 최대 55%까지 향상되었고, 사지 고정과 인간 유래 근세포 모델에서도 동일한 효과가 재현돼 임상적 적용 가능성을 뒷받침했다.
이번 연구는 DUSP22가 근육 위축을 유도하는 병리적 기능을 세계 최초로 규명하고, 이를 표적으로 한 약물 전략이 근감소증뿐 아니라 다양한 근육 퇴행성 질환 치료에도 활용될 수 있음을 보여준다. 연구팀은 이번 성과가 근육 소실의 기전을 이해하고, 근감소증 치료제를 개발하는 전환점이 될 것으로 평가했다. 연구 결과는 국제학술지《EMBO Molecular Medicine》에 게재됐다.